Reformulación de medios de cultivo en los procedimientos del Archivo de Bogotá para optimizar el crecimiento microbian
Reformulación de medios de cultivo en los procedimientos del Archivo de Bogotá para optimizar el crecimiento microbian
Por: mllaiton
Publicado el: Septiembre 2023
Por Pablo Vanegas. Profesional Universitario Subdirección de Gestión del Patrimonio Documental
Dentro de las funciones que tiene el Archivo de Bogotá se encuentra la de garantizar la preservación de la historia y memoria institucional, para lo cual se realizan procedimientos enfocados a la la conservación de la documentación. Uno de estos, está direccionado hacia la eliminación de las posibles afectaciones, documentales y al personal que lo manipula, causadas por microorganismos dentro de lo cual se utilizan medios de cultivo que ayudan en la individualización y en ocasiones identificación de posibles agentes patógenos. En la actualidad, los medios de cultivo utilizados son los que fueron reportados desde años atrás, y hasta la fecha no se han tenido en cuenta posibles avances en estos que puedan ayudar a mejorar la eficiencia de los procesos. Es por esto que se realizan estudios comparativos, con medios de cultivo comerciales, que incrementen la identificación de microorganismos.
Para adelantar el estudio se seleccionaron los siguientes medios teniendo en cuenta las características que presentaban y los posibles beneficios para el desarrollo del objetivo.
Agar Caseinato Cálcico: Se utiliza para la identificación de bacterias proteolíticas, esto debido a la formulación del medio que permite visualizar un halo transparente en aquellas colonias que poseen esta capacidad
Agar Czapeck: se usa comúnmente para el cultivo de hongos y la formación de clamidosporas por C. albicans. Para el cultivo de organismos acidófilos, como las levaduras, la acidez del medio puede aumentar. También se usa para estudios taxonómicos de Aspergillus, Penicillium y Actinomycetes.
Agar OGYE: Es un medio selectivo recomendado para el aislamiento y enumeración de levaduras y mohos en productos alimenticios. También puede ser utilizado con muestras de origen clínico y cosmético.
Agar Extracto de Malta: Es un medio recomendado para el aislamiento, detección y enumeración de hongos y levaduras. También puede emplearse como una prueba de esterilidad para detectar la presencia de estos organismos.
Agar Extracto de Levadura: es un medio rico en nutrientes que permite la recuperación de un amplio espectro de bacterias, levaduras y mohos. Este medio es recomendado por ISO 6222 para el recuento en placa de microorganismos en todo tipo de aguas.
Agar ADP: El Dextrosa de papa se utiliza comúnmente en la detección de hongos, en la actualidad es el utilizado en el escobilleo sobre el material documental.
Agar Rosa de Bengala Cloranfenicol: Se utiliza para el aislamiento selectivo y la enumeración de levaduras y mohos de materiales y alimentos ambientales. El medio contiene peptona micológica que actúa como fuente de carbono, nitrógeno, minerales, vitaminas y otros nutrientes esenciales para el crecimiento.
Agar Nutritivo: Formado por peptona, extracto de carne bovina y agar. Esta fórmula relativamente sencilla proporciona los nutrientes necesarios para la multiplicación de un amplio número de microorganismos que no son necesariamente exigentes.
Sobre estos medios se realizó crecimiento de microorganismos a partir de escobilleo sobre material documental contaminado (fig.1), y recolecta de muestras ambientales (500 L) con equipos muestreadores de aire MAS 100.
Figura 1: Soportes documentales pertenecientes al fondo CINEP del cual se toma el material microbiano de partida para los ensayos de crecimiento.
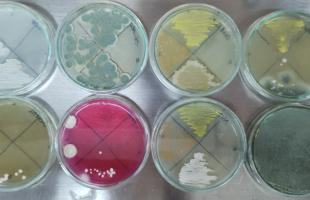
En general, las muestras y los escobilleos de cepas individualizadas, no presentaron una tendencia a aumentar en alguno de los medios utilizados, además se presentó que para una misma cepa se presentaban morfologías evidentemente distintas, de acuerdo con el medio en el que crecía (fig. 2). Por otra parte, la diversidad y la cantidad de unidades formadoras de colonia no fueron favorecidas por algún medio en específico.
Figura 2: Medios de cultivo sólido sobre el cual se realizó escobilleo de 4 distintas cepas microbianas.
Conclusión
No es posible determinar un único medio de cultivo que cumpla con las expectativas de los objetivos del estudio, para esto se podría pensar en hacer una toma de muestra sobre varios de estos para obtener la mayor cantidad de información y que satisfaga tanto la diversidad como las UFC a encontrar.
Al existir diferencias en la morfología de un mismo organismo dependiendo de los sustratos tomados para su crecimiento se podrían presentar dobles conteos si se llegara a realizar lo descrito en el párrafo anterior, para lo cual se debe tener bien identificado cómo los distintos grupos de organismo se comportan en los distintos medios de cultivo.
Este estudio, al haber sido realizado sobre microorganismos tomados al azar de muestras de documentación contaminada y ambientales, no pudo restringir las variables implícitas dadas por la cantidad y diversidad microbiana, es por esto que se requiere hacer un estudio similar utilizando muestras previamente individualizadas.
Bibliografía
Albaum S, Masaphy S. Comparison of rose bengal-chloramphenicol and modified aureomycin-rose bengal-glucose-peptone agar as media for the enumeration of molds and yeasts in water by membrane filtration techniques. J Microbiol Methods. 2009 Mar;76(3):310-2. doi: 10.1016/j.mimet.2008.11.006. Epub 2008 Dec 13. PMID: 19111583.
Beuchat LR. Selective media for detecting and enumerating foodborne yeasts. Int J Food Microbiol. 1993 Jun 25;19(1):1-14. doi: 10.1016/0168-1605(93)90119-2. PMID: 8357752.
Böllmann J, Martienssen M. Comparison of different media for the detection of denitrifying and nitrate reducing bacteria in mesotrophic aquatic environments by the most probable number method. J Microbiol Methods. 2020 Jan;168:105808. doi: 10.1016/j.mimet.2019.105808. Epub 2019 Dec 12. PMID: 31837971.
Caycedo Lozano, Liliana, Ramírez, Lucía Constanza Corrales, & Suárez, Diana Marcela Trujillo. (2021). Las bacterias, su nutrición y crecimiento: una mirada desde la química. Nova, 19(36), 49-94. Epub January 17, 2021.https://doi.org/10.22490/24629448.5293
López De Volder, María A., Pioli, Verónica, Breglia, Noelia, Teves, Sergio, & Degrossi, José. (2019). Comparación de medios de cultivo selectivos para el aislamiento de especies del Taxón K perteneciente al complejo Burkholderia cepacia. Ars Pharmaceutica (Internet), 60(2), 93-100. Epub 28 de junio de 2019.https://dx.doi.org/10.30827/ars.v60i2.8312